
Notre corps se dégrade inexorablement, plus ou moins vite, et nous ne savons pas vraiment pourquoi. Néanmoins, la connaissance croissante des processus du vieillissement ouvre de vastes horizons, au point qu’on a déjà pu l’inverser chez l’animal et jusque dans des cellules humaines.
La recherche en la matière a fait d’énormes progrès ces dernières décennies. Elle découvre, de plus en plus finement, les mécanismes du vieillissement au coeur de nos cellules et de notre ADN, qui se traduit sur notre forme et notre apparence. Essayons d’expliquer au profane, ces données fondamentales qui pourraient changer notre avenir et/ou celui de nos enfants.
Plus de 300 théories ont été émises (1) et il semble que vieillir soit bien complexe, et puisse avoir de nombreuses causes. Globalement, notre vieillissement entraîne une baisse de notre fertilité et de nos défenses immunitaires, avec une sensibilité accrue aux maladies. Nos cellules et nos tissus fonctionnent moins bien, ainsi nos organes sont moins performants, et notre santé se dégrade. Le risque de mortalité augmente. Mais pourquoi ?
Vous trouverez ici les théories sur les causes (ou en tout cas des mécanismes) du vieillissement les plus retenues aujourd’hui. Rien n’est vraiment sûr. La science nous en apprend régulièrement plus, et l’on revient parfois aussi en arrière sur certaines théories.
Il est encore difficile de faire la différence entre les effets constatés du vieillissement et ses causes, surtout au niveau cellulaire.
Les scientifiques retiennent que, globalement, une accumulation d’éléments cellulaires détériorés se fait au fil du temps (en particulier des parties de notre ADN et des mitochondries* de nos cellules). Ces détériorations sont dues à l’environnement (radiations, toxiques, carences, stress divers…) ou à des problèmes internes (erreurs de réplication des cellules, oxydation, inflammation…).
Les cellules fonctionnent alors mal, elles « vieillissent ». Lorsqu’elles sont trop endommagées, elles peuvent au mieux s’auto-détruire (par apoptose: une espèce de suicide cellulaire). Sinon, elles peuvent rester « anormales », et c’est entre autres, une voie vers le cancer. Elles peuvent aussi devenir des cellules sénescentes qui ne se reproduisent plus, n’ont plus leur fonctions normales, deviennent encombrantes et secrètent des substances toxiques pour les cellules voisines, entraînant de l’inflammation dans ces tissus qui vieillissent.
Le corps cherche à éliminer ces cellules non fonctionnelles grâce à son système immunitaire. Hélas, l’âge avançant, ce dernier s’affaiblit.
Les dernières recherches étudient comment éliminer ces cellules sénescentes, ce qui paraît une voie majeure en anti-âge, tout comme la reprogrammation épigénétique que nous verrons plus bas, et qui consiste en une sorte d’inversion du vieillissement cellulaire.
L’accumulation de détériorations dans les cellules de notre corps
L’oxydation et les radicaux libres
C’est une des théories majeures, proposée par le chimiste Denham Harman dès 1956, bien que récemment, on soit revenu sur l’usage systématique des antioxydants contre le vieillissement. Ce n’est pas si simple. Néanmoins, l’oxydation reste un phénomène très impliqué dans la détérioration des tissus du corps et dans les maladies liées au vieillissement (3).
 Tels le morceau de fer qui rouille, nos tissus s’oxydent naturellement avec le temps. L’oxydation est le résultat des processus de « combustion » et de réactions métaboliques normales qui produisent des radicaux libres comme une chaudière produit des gaz nocifs. Cette production vient essentiellement de nos mitochondries, les génératrices d’énergie au sein de nos cellules.
Tels le morceau de fer qui rouille, nos tissus s’oxydent naturellement avec le temps. L’oxydation est le résultat des processus de « combustion » et de réactions métaboliques normales qui produisent des radicaux libres comme une chaudière produit des gaz nocifs. Cette production vient essentiellement de nos mitochondries, les génératrices d’énergie au sein de nos cellules.
Nous avons des systèmes antioxydants qui permettent de limiter les dégâts mais ceux-ci peuvent être vite dépassés. A la longue, les radicaux libres peuvent altérer de plus en plus nos tissus et créer des protéines, voire des cellules, anormales, une dénaturation des lipides, de notre ADN, etc…
Il a été démontré de nombreuses fois que les antioxydants pouvaient avoir des effets positifs sur des maladies liées au vieillissement. Cependant, la durée de vie n’est pas vraiment rallongée par les antioxydants, et certaines études ont même constaté le contraire dans certains cas. Il apparaît que la production de radicaux libres par nos mitochondries soit capable d’enclencher justement des mécanismes de survie ou de réparation cellulaires. Il ne faut donc pas systématiquement augmenter les niveaux d’antioxydants.
A l’inverse, lorsque le corps est dépassé par cette production, ou que des radicaux libres « externes » sont apportés par l’environnement ou la nourriture, et que la « réaction en chaîne » d’oxydation se propage, les antioxydants seront utiles. Une fois de plus, tout est question de mesure, et la voie du milieu parait toujours la plus sage. Rien n’est tout blanc, rien n’est tout noir.
La détérioration des mitochondries
Cette autre théorie de D. Harman prend plus d’importance depuis les dernières avancées scientifiques. Les mitochondries (en moyenne quelques centaines par cellule) ont le rôle primordial de générer l’énergie pour leur fonctionnement et donc, celui de notre corps. Ces « petites chaudières » brûlent en permanence des nutriments (principalement du glucose, mais pas que…) avec de l’oxygène.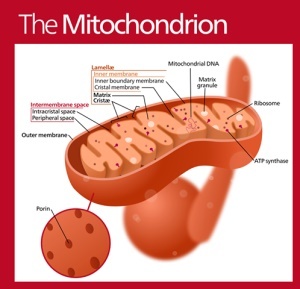
Les réactions d’oxydation de cette combustion produisent beaucoup de radicaux libres qui, s’ils sont en excès, peuvent détériorer la mitochondrie elle-même (elle est en première ligne), et plus tard, l’ADN de la cellule, sa membrane ou d’autres éléments…(4)
Dans ce cas, la production d’énergie baisse et les réactions métaboliques aussi. Les cellules concernées fonctionnent moins bien, tout comme les tissus et les organes qu’elles constituent. Si l’état mitochondrial continue de se dégrader, la cellule sera amenée à s’autodétruire par « apoptose » dans le meilleur des cas. Sinon, elle pourra devenir une cellule sénescente qui encombrera inutilement nos tissus, les faisant devenir vieux.
Il a été décrit une altération de la production d’énergie cellulaire avec l’âge ainsi qu’une détérioration accrue des mitochondries lors de carences en certains minéraux et vitamines. Récemment, on a montré que cette détérioration survenait notamment lors du manque d’un coenzyme : le NAD+, proche de la vitamine B3). Celui-ci est très impliqué dans la production d’énergie de la cellule et il diminue avec l’âge. Une autre piste à suivre…
La détérioration des protéines et la glycation
Les protéines sont les éléments qui structurent notre corps, notre ADN, qui forment nos enzymes, nos hormones, etc… Avec l’âge, nos cellules peuvent fabriquer des protéines de forme inadéquate qui deviennent alors inopérantes.
D’autre part, elles peuvent se combiner à d’autres molécules, ce qui les rend aussi moins fonctionnelles, et conduit à une altération des cellules et des tissus. La glycation (voir ici) est une combinaison particulière se faisant entre nos protéines et des glucides (sucres). Les tissus les plus touchés sont, comme chez les diabétiques, les parois des vaisseaux, la rétine, et surtout le collagène donnant la fermeté à la plupart des tissus du corps… Ils perdent leur souplesse, entre autres effets délétères. La tendance au durcissement des fibres de collagène fait que les échanges et la nutrition des cellules sont globalement ralentis. Un milieu corporel trop acide favoriserait ces combinaisons.
La réduction des sucres et aliments faisant fortement monter la glycémie est une façon de limiter la glycation.
Les erreurs de réplication des cellules et la détérioration de notre ADN
 Des petites anomalies peuvent se retrouver après un certain nombre de multiplications des cellules de notre corps. De plus, notre ADN subit une détérioration quotidienne par les facteurs environnementaux chimiques ou physiques (entre 1000 et 1 000 000 lésions par cellule, qu’elle devra réparer).
Des petites anomalies peuvent se retrouver après un certain nombre de multiplications des cellules de notre corps. De plus, notre ADN subit une détérioration quotidienne par les facteurs environnementaux chimiques ou physiques (entre 1000 et 1 000 000 lésions par cellule, qu’elle devra réparer).
Aujourd’hui, certains gènes sont connus comme pouvant influencer notre durée de vie (ralentir le vieillissement), et sont en fait impliqués dans la réparation de l’ADN. Malgré ce système de correction/réparation dans nos cellules, une accumulation des erreurs peut conduire, à la longue, au mauvais fonctionnement de nos cellules, à la dégénérescence, la sénescence ou la mort de celles-ci, puis à la nôtre.
Le raccourcissement progressif des télomères
Les télomères sont un genre de capuchon protecteur des extrémités de nos chromosomes (brins d’ADN). Leur taille diminue au fil des divisions cellulaires et donc avec l’âge. La division cellulaire permet aux tissus de se maintenir ou se régénérer, comme la peau se reforme après une blessure.
On pense qu’après la disparition des télomères, ce sont des gènes des chromosomes qui peuvent être détruits à leur tour, par manque de protection, entraînant ainsi la mort des cellules ou la production de cellules sénescentes ou anormales, que le corps devra éliminer.
Hayflick avait montré qu’il y avait une limite au nombre de divisions des cellules (une cinquantaine). Il semble que la découverte de l’usure des télomères explique cela. En revanche, pour certaines « cellules souches » la limite irait bien au delà (jusqu’à 1000 fois). En fait, ces dernières fabriquent une enzyme (la télomérase) découverte récemment, et qui peut « réparer » ce raccourcissement des télomères. A priori, elle est fabriquée chez le foetus mais pas chez l’adulte (sauf par les cellules cancéreuses, qui se multiplient à l’excès, et nos fameuses cellules souches).
Cependant, la théorie est loin d’être parfaite, et de tout expliquer. Depuis, les scientifiques ont constaté que ce fonctionnement peut être différent selon le type de cellules du corps, ou selon les espèces par exemple. La corrélation de télomères longs avec la longévité des cellules n’est pas systématique.
La longueur des télomères serait plutôt un marqueur du vieillissement qu’un facteur. Un raccourcissement important est lié à de mauvaises défenses immunitaires, aux maladies de dégénérescence, et au stress permanent… mais il n’en est pas directement la cause. Voir ici télomères et télomérase >
Un système de réparation cellulaire moins efficace
Tous les phénomènes cités ci-dessus détériorent nos cellules et s’accentuent avec le temps. Ces cellules possèdent bien des mécanismes de réparation mais ils deviennent moins efficaces. Un d’entre eux, appelé « autophagie » est majeur, et mieux connu depuis quelques années seulement. Son déclin pourrait être un des principaux facteurs du vieillissement. La bonne nouvelle est qu’on peut le stimuler, tout comme les autres fonctions de réparation d’ailleurs.
Nous venons donc de voir qu’une notion de dommages accumulés dans nos cellules, tissus et organes se dégage de ces théories, associées à une baisse d’efficacité des processus de réparation sans laquelle nous ne vieillirions quasiment pas. C’est d’ailleurs le cas de certains animaux que nous ne détaillerons pas ici.
L’encrassement toxinique
Dans nos cellules et autour d’elles, des résidus métaboliques (déchets) ou des polluants externes s’accumulent et peuvent empêcher leur fonctionnement normal.
La lipofuscine, notamment, est un produit de dégradation de protéines que les cellules n’arrivent plus bien à « digérer » et à éliminer au fil du temps. Des dépôt de lipofuscine intracellulaire augmentent avec l’âge dans de nombreux tissus. Ils participent, par exemple, à la formation des taches brunes de la peau qui vieillit. Ils peuvent générer des maladies pour les cellules du corps qui se multiplient pas ou peu (comme les cellules musculaires et nerveuses) donc pour le coeur et le cerveau. On les retrouve en très grande quantité dans les cellules du cerveau atteint d’Alzheimer.
De même, ces substances toxiques peuvent s’accumuler entre les cellules (milieu intercellulaire), empêchant alors les échanges qui assurent l’apport nutritif des cellules et la bonne élimination de leurs déchets. C’est notamment le cas des dépôts amyloïdes dont on connaît les fameuses « plaques amyloïdes », abondantes dans le cerveau des personnes atteintes d’Alzheimer. Il s’agit des plus importants déchets protéinés issus des cellules qui ont tendance à s’agglutiner. Leur présence ralentit alors de plus en plus les échanges nutritifs (du sang vers les cellules) et le drainage des toxines (des cellules vers le sang). La communication entre cellules se fait aussi de moins en moins bien.
On sait que les phénomènes auto-immuns, l’inflammation, la glycation, la pollution par les métaux lourds et des taux trop bas de vitamine D, favorisent ces dépôts extracellulaires mais on n’en connaît pas les causes exactes. En tous cas, ils favorisent des dommages sur notre ADN, qui, à leur tour, favorisent le vieillissement.
Diminution de la méthylation
La méthylation est une réaction biologique qui diminue globalement avec l’âge. Ainsi, certaines fonctions utiles à la santé vont se ralentir progressivement. Par exemple, les fonctions de réparation de notre ADN ou de nos cellules, et bien d’autres…
Les scientifiques pensent que la diminution de la méthylation est corrélée avec le vieillissement et de nombreuses maladies de dégénérescence.
Une bonne méthylation est liée à des télomères plus longs (marqueurs de longévité).
Hélas rien ne précise vraiment pourquoi elle diminue en vieillissant. En revanche, il est toujours possible à veiller aux conditions nécessaires à ce processus de méthylation voire à l’améliorer.
Epuisement des cellules souches
 Les cellules souches sont capables de se diviser pour donner naissance à des cellules neuves spécifiques d’un organe particulier (par exemple : cellules du foie, de la peau, des muscles…). On les croyait seulement chez l’embryon, il n’y a pas si longtemps. Aujourd’hui, on sait qu’elles sont présentes en très faibles quantités chez l’adulte, dans ses tissus. Certaines permettent de générer un seul type de cellules ou pour un seul organe, d’autres (dites « pluripotentes ») peuvent générer divers types de cellules.
Les cellules souches sont capables de se diviser pour donner naissance à des cellules neuves spécifiques d’un organe particulier (par exemple : cellules du foie, de la peau, des muscles…). On les croyait seulement chez l’embryon, il n’y a pas si longtemps. Aujourd’hui, on sait qu’elles sont présentes en très faibles quantités chez l’adulte, dans ses tissus. Certaines permettent de générer un seul type de cellules ou pour un seul organe, d’autres (dites « pluripotentes ») peuvent générer divers types de cellules.
Leur nombre, plus important chez l’enfant, diminue avec l’âge. En vieillissant, on constate que le renouvellement cellulaire se ralentit. A l’inverse, le nombre de cellules sénescentes ou anormales augmente, comme nous l’avons vu plus haut. Les organes deviennent moins performants.
Des recherches ont permis d’améliorer la longévité d’animaux en augmentant le nombre de leurs cellules souches par certains traitements ou par manipulations génétiques. Notons cependant qu’il s’agit de traitements qui sont loin de faire l’unanimité et potentiellement dangereux car une mutation d’ADN dans les cellules souches peut facilement amener un état pré-cancéreux de ces dernières.
Par ailleurs, les études récentes tendent à relier cette dégradation des cellules souches à celle de leurs mitochondries, ce qui rejoint la théorie du vieillissement mitochondrial (Pr Hongbo Zhang 2016).
Le vieillissement et la mort programmés dans nos gènes
Notre horloge biologique
Selon cette théorie, notre durée de vie serait fixée par une sorte d’horloge biologique cellulaire, ce qui irait dans le sens de la survie de l’espèce humaine. Ici, il s’agirait d’un programme allant de la conception à la mort de l’individu. Notre vieillissement commence à notre naissance.
Avec l’évolution, certains gènes auraient été sélectionnés car il vont dans le sens de la survie et de la reproduction (conservation de l’espèce) mais ils pourraient avoir un effet délétère sur la longévité plus tard en vieillissant (c’est la théorie de G.C. Williams au nom barbare de « pléiotropie antagoniste »).
Les sujets âgés, ayant pu assumer leur reproduction pendant leur jeunesse, et devenant moins utiles à l’espèce (voire encombrants sur le plan de la survie du groupe), il est possible que la nature ait retenu un plan d’extinction programmée des plus vieux…
N’oublions pas que, très récemment encore pour l’espèce humaine (quelques dizaines de milliers d’années), le mode de vie, l’environnement et ses dangers permanents faisaient que peu de sujets atteignaient les 40 ou 50 ans. L’évolution n’a probablement pas eu le temps de s’adapter au changements qui font qu’aujourd’hui on vit bien plus longtemps en moyenne.
Par exemple, on sait maintenant que la fabrication d’hormone de croissance (GH) favorise de beaux muscles mais peut réduire la longévité. C’est une fonction utile pour la survie et la reproduction mais pas pour vivre longtemps.
Le dérèglement épigénétique
Récemment, des études apportent un jour nouveau à cette théorie, et confirmeraient son intérêt. Il s’agit des changements épigénomiques.
Pour faire simple, disons que certains de nos gènes sont impliqués dans les processus de vieillissement (le ralentissant ou l’accélérant selon les gènes). Notre corps peut (sous certaines conditions) les activer ou les inactiver (notamment par des réactions de méthylation, voir l’épigénétique), déclenchant ou pas certaines fonctions liées au vieillissement. Selon les fonctions activées, cet ensemble de gènes peut alors influencer le processus du vieillissement cellulaire dans un sens ou dans l’autre.
Par exemple, les hormones du stress telles que le cortisol peuvent entraîner des changements épigénétiques sur l’ADN de nos cellules, accélérant ainsi l’horloge du vieillissement.
Mais l’épigénétique est aussi une voie majeure que nous pouvons contrôler pour améliorer la longévité.
On connaît déjà beaucoup de ces mécanismes et des moyens de les moduler pour « ralentir » le vieillissement. Il reste à savoir précisément pourquoi, sans intervention, tout cela va inéluctablement dans le sens du vieillissement…
Peut-on remettre l’horloge de notre corps à zéro ?
Les découvertes sur les télomères (voir plus haut), la méthylation de l’ADN (qui peut modifier l’activité de nos gènes), les sirtuines, et la reprogrammation épigénétique, pourraient confirmer cette hypothèse.
En fait, toutes les cellules de notre corps contiennent le même ADN. La différence entre une cellule souche et une cellule de foie, de peau, d’os… ne tient qu’à la conformation de notre ADN (en gros : la façon dont notre ADN est replié et compacté sur lui-même) et qui peut se modifier. C’est ce qu’on appelle le programme épigénétique de la cellule. Les gènes restant strictement les mêmes, c’est seulement leur expression qui changerait en vieillissant.
On sait qu’avec l’âge des changements épigénétiques souvent délétères s’accumulent. Leur observation sur certains emplacements de l’ADN peut aujourd’hui prédire la longévité d’un individu de façon assez fiable. Il existe des tests d’âge biologique épigénomiques à partir d’un échantillon de sang. Ces changements le plus souvent liés à des « méthylations » modifient le programme épigénétique mais pas les gènes eux-mêmes. A l’inverse, elles peuvent être défaites (déméthylations), améliorant notre épigénome, renversant alors le vieillissement de la cellule (par exemple restriction calorique, activité physique, ou expérimentations diverses… en sont capables).
 Les études ayant débouché sur un allongement de la durée de vie (chez les animaux) sont nombreuses malgré cette horloge qu’on ne semble pas pouvoir arrêter. Dans les faits, un corps humain, jusqu’à 50 ans au moins, sait fabriquer des cellules saines et jeunes, sans aucun signe de vieillissement : lors de la procréation, deux corps faits de cellules ayant plusieurs décennies (présentant donc un certain vieillissement) sont capables de créer une cellule complètement jeune et qui deviendra leur enfant.
Les études ayant débouché sur un allongement de la durée de vie (chez les animaux) sont nombreuses malgré cette horloge qu’on ne semble pas pouvoir arrêter. Dans les faits, un corps humain, jusqu’à 50 ans au moins, sait fabriquer des cellules saines et jeunes, sans aucun signe de vieillissement : lors de la procréation, deux corps faits de cellules ayant plusieurs décennies (présentant donc un certain vieillissement) sont capables de créer une cellule complètement jeune et qui deviendra leur enfant.
Sans cela, notre espèce dépérirait rapidement ! Il a été montré que l’ovocyte de la femme contenait ces facteurs rajeunissants. Hélas, personne n’a encore pu les utiliser en pratique…
En revanche, il est théoriquement possible d‘inverser certaines expressions de gènes liés au vieillissement. L’enjeu incroyable serait donc de pouvoir faire revenir certains tissus ou organes à un état antérieur, « rajeunis ».
Ceci a déjà été fait sur l’animal et sur des cellules humaines que l’on a rajeuni, jusqu’à leur stade primaire de cellule souche pluripotente.
Il apparaît aujourd’hui que le vieillissement des cellules correspond aussi à des modifications épigénétiques s’installant peu à peu dans ce programme. En théorie au moins, cela serait partiellement réversible comme l’affirment des chercheurs très avancés (p.ex. Pr David Sinclair ou Pr Jean-Marc Lemaitre (8)(9)). Des études l’ont confirmé.
C’est la reprogrammation épigénétique des processus de vieillissement, qui consiste donc à ramener les cellules vers un stade antérieur (plus jeune), voire jusqu’à la cellule souche qu’elles étaient à l’origine. L’avantage certain est qu’il n’y a pas ici de modification génétique. Rappelons que l’ADN et les gènes resteraient indemnes. Vaste programme tout de même !
Pour l’heure, des résultats sont obtenus avec des technologies très pointues et non dénuées de risques (injection de rétrovirus, utilisation de thérapies géniques…). Elles sont encore loin de l’utilisation médicale courante, même si des chercheurs le prévoient dans les 10 ans à venir.
Vieillissement et médecines traditionnelles
 La médecine chinoise dit qu’une quantité d’énergie vitale dite « ancestrale » naît de la fusion de l’ovule et du spermatozoïde. Elle nous est donnée à la naissance, et ne peut pas se renouveler. Lorsque celle-ci est épuisée, la vie se termine.
La médecine chinoise dit qu’une quantité d’énergie vitale dite « ancestrale » naît de la fusion de l’ovule et du spermatozoïde. Elle nous est donnée à la naissance, et ne peut pas se renouveler. Lorsque celle-ci est épuisée, la vie se termine.
En Ayurveda, vieillir est un phénomène naturel mais auquel on peut pallier avec divers soins et comportements pour se maintenir au mieux. Toute une branche de l’Ayurvéda y est consacrée, prenant en compte notamment l’élimination des toxines, la nutrition, la respiration… Cependant, le temps fait partie intégrante de toute création, comme si un potentiel était défini et donné à la naissance de chaque être vivant.
Seules des pratiques de yoga et de samadhi (étape « d’éveil ») pourraient permettre à des personnes à haut niveau de conscience d’y échapper ce qui ne serait quasiment pas possible dans le monde actuel (6).
Tout ceci rejoint une des plus récentes théories sur la cause du vieillissement (dite du « soma jetable » de Thomas Kirkwood), où les ressources vitales seraient limitées. Le corps les distribuerait entre les fonctions de reproduction (essentielles pour la survie de l’espèce) et l’entretien des autres tissus du corps (le soma). Ainsi, dans le règne animal on constate généralement que : plus la reproduction se fait tôt et plus la progéniture est nombreuse, moins la durée de vie est longue, puisqu’elle n’apporte rien à la survie de l’espèce.
En conclusion
Dans le même temps, alors que notre organisme sait réparer la plupart de ces anomalies, il ne le fait plus correctement, notamment en raison de ces modifications du programme épigénétique survenant avec l’avancée en âge, qui vont entraver le bon fonctionnement des gènes de réparation et d’autres…
Reste à savoir pourquoi se font ces modifications : hasard statistique, usure, imperfection ou volonté parfaite de la nature…? Il se peut bien que certaines données échappent définitivement à une science trop matérialiste.
Connaître à présent la possible réversibilité de certaines de ces modifications (au moins jusqu’à un certain point) est certes une grande avancée scientifique. Espérons qu’il en sera fait bon usage, ce qui est une autre histoire.
En attendant, sachant que le mode de vie et l’environnement peuvent modifier largement l’expression de nos gènes, et donc ce programme épigénétique, nous pouvons déjà en profiter avec des techniques mettant en jeu la nutrition, l’autophagie, l’hormèse, certaines substances naturelles, etc… destinées à nous renforcer, et qui sont décrites dans le présent site.
Voyez les effets du vieillissement sur votre corps >
Bibliographie :
(1) MEDVEDEV Z. A., « An attempt at a rational classification of theories of ageing », Biological reviews of the Cambridge Philosophical Society, vol. 65, 1990, p. 375-398.
(2) PEARL R., The Rate of Living : Being an Account of Some Experimental Studies on the Biology of Life Duration, New York, A. A. Knopf, 1928
(3) HARMAN D., « Aging : a theory based on free radical and radiation chemistry », Journal of gerontology, vol. 11, 1956, p. 298-300
(4) BALABAN R. S., NEMOTO S. et FINKEL T., « Mitochondria, oxidants, and aging », Cell, 2005. vol. 120, p. 483-495
(5) Lapasset L, Milhavet O, Prieur A, Besnard E, Babled A, Aït-Hamou N, Leschik J, Pellestor F, Ramirez JM, De Vos J, Lehmann S, Lemaitre JM. Rejuvenating senescent and centenarian human cells by reprogramming through the pluripotent state. Genes Dev. 2011 Nov 1;25(21):2248-53. doi: 10.1101/gad.173922.111. PMID: 22056670; PMCID: PMC3219229
(6) Sastri K, Chaturvedi G, editors. Sarirasthan. Varanasi: Chaukhamba Bharti Academy; 1998. Agnivesha, Charak Samhita, Vidyotini; p. 834.
(7) KIRKWOOD T. B. L., « Evolution of ageing », Nature, vol. 270, 1977, p. 301-304.
(8) * Ferry Luc; Lemaître Jean-Marc. Guérir la vieillesse. Ed. Humensis.
(9) * David Sinclair. Pourquoi vieillit-on ? Ed. Quanto



article passionnant. quel beau travail. merci encore docteur. je decouvre tous vos texte sur ce site avec delectation
Merci. Tout le plaisir est pour moi si tout cela vous intéresse. Bonne lecture et soyez en forme.
BIZARRE,
QUAND J’AVAIS 20 ANS MON CORPS AVAIT L’AIR D’UNE JEUNE FILLE DE 12 ANS. AUJOURD,HUI, J’AI 67 ANS ET JE SUIS EN PLEINE FORME. JE MARCHE 3 FOIS PAR JOUR ET MON CORPS ME DONNE 45-50 ANS. TOUT LE MONDE ME LE DIT. ETANT JEUNE J’AI EU UN PROBLEME AVEC LA MOELLE ÉPINIERE. PEUT-ETRE QUE CELA A JOUER SUR MON CORPS. AUCUNE IDÉE.
Bonjour, j’aime beaucoup votre façon de voir les choses. On lit souvent que les causes du vieillissement sont l’inflammation, un mauvais microbiote, la baisse des hormones etc. Mais je crois comme vous que ce sont des conséquences et non pas des causes du vieillissement, et elles nous enmènent ensuite vers la maladie. Les vraies causes (ou la cause des causes…) sont certainement plus profondes en ancrées dans nos cellules. Peut-être même suivent elles une logique que l’on ne veut pas vraiment voir…
Merci pour votre commentaire.
Oui, d’après certains scientifiques, on ne connaîtrait que 4% des lois de ce monde. En médecine et en biologie, plus on explore et plus on découvre des mécanismes et des facteurs de plus en plus subtils mais il cela semble sans fin. Vous avez raison, il y a peut-être dans tout cela une logique qui nous dépasse, invisible mais omniprésente. Qui sait ? ;-)
Une médecine traditionnelle comme l’Ayurvéda a une vue plus globale des choses. Elle n’a pas besoin d’analyser chaque détail et elle inclue aussi le spirituel. On aurait certainement intérêt à s’y pencher un peu plus en occident.
Merci pour votre synthèse. Vous êtes un remarquable pédagogue et donc, en ce qui me concerne, c’est très inspirant, et cela devrait l’être pour des personnes à la recherche d’un chemin pour atterrir vieux plus intelligemment.
Ce serait intéressant d’aborder de façon aussi synthétique et pédagogique la grande ambition de la médecine fonctionnelle (filière américaine, c’est-à-dire inclusive).
Merci beaucoup. Ravi que ce thème un peu « technique » vous inspire.
Je crois que l’approche de la médecine intégrative ou bien celle de la médecine fonctionnelle inclusive sont très proches dans la mesure où elles essaient toutes deux de remonter au maximum vers l’origine profonde des maladies (ou des symptômes), et considèrent l’individu dans son ensemble. En tout cas, c’est ce que j’essaie de communiquer à mon humble niveau, sur le thème du bien vieillir.
Superbe article… Ainsi l’Homme peut mieux connaître son corps en lisant ce site… et en suivant ses conseils… En fait l’homme (d’une manière générale) a perdu le temps de s’occuper de lui, du moins autant que de sa voiture, de ses meubles, ou de ses objets connectés. Quand on pense que, chaque minute, plus de cent millions de cellules naissent et meurent, que nous devons « entretenir » nos plus de cent mille kilomètres d’artérioles et de veinules, qu’il se reconstruit entièrement en deux ans (vitesses variables selon les tissus), on ne peut être qu’ébahi et tout faire pour le maintenir en bon état de marche. Des phénomènes quantiques se produisent également dans notre corps (biophysique) à l’image notamment des microtubules, ce squelette cellulaire qui se crée à très grande vitesse, attribuant une place dans l’espace cellulaire pour ses organites et faisant en sorte que les métabolismes idoines soient assurés. Et l’esprit est aussi important que le corps physique pour une bonne santé. Voir notamment https://www.antiageintegral.com/forme/entre_corps_et_esprit et d’aitres articles sur le site. Portez vous bien !
Merci Roger. Oui quand on réfléchit quelques instants à ce qui se passe dans une cellule de notre corps, ou à la fabrication d’un embryon à partir de quelques cellules, et de ce qui fait que la croissance des organes s’arrête exactement là où il faut, etc… c’est grisant. On ne peut que se poser la question de savoir quel est le moteur de tout cela. Et ça pourrait bien être le même qui gère notre vieillissement… Il y a beaucoup matière à méditer la dessus.
Merci pour ce bel article très fouillé et hyper intéressant. Le longévité en bonne santé ne semble pas être pour moi! Alors que je me suis toujours correctement alimentée, fait du sport, gardé le moral et la motivation, j’ai développé depuis 2015 une maladie auto immune (sclérodermie systémique) extrêmement grave (atteinte pulmonaire, cardiaque, foie, oesophage …etc)
Je m’alimente du mieux possible, fait du sport tous les jours, garde un moral à tout épreuves
Je vais avoir 74 ans
Que puis je faire ?
Bonne soirée
Merci pour votre appréciation. Il ne serait pas sérieux de vous donner ici la conduite à tenir dans votre cas particulier. La sclérodermie est une affection handicapante et je vous souhaite qu’elle s’améliore. Votre bonne hygiène de vie ne pourra qu’aider. Cette maladie n’est pas spécifiquement liée au vieillissement. Certaines formes débutent très tôt.
Comme pour la plupart des maladies auto-immunes, vous pourriez peut-être vérifier du côté de votre intestin, microbiote et perméabilité intestinale, avec un médecin compétent. Bien à vous.
wow! belle synthèse cher confrère. j’ai beaucoup appris. Pour ma part je pense que rester en forme jusqu’au bout est déjà un très beau challenge au lieu de dépérir lentement pendant des décennies. Allonger la vie après 100 ou 110 ans, je crois qu’il y a quelque chose qui nous dépasse là dedans et que les chercheurs pourraient bien s’y fourvoyer!
Merci bien. je suis 100% d’accord avec vous. Comme je l’ai écrit plus haut, l’approche trop matérialiste du vieillissement pourrait bien mener les chercheurs vers une impasse. Qui sait ?
avoir une vie calme se nourrir modérément sans se gaver essayer de préparer des repas sains l huile d olive m a toujours accompagnée meme sur la peau le miel bio est un médicament il a contribué à la guérison d un ulcère le soir avant de dormir une cuillère à soupe et ne pas boire derrière bien sûr les tisanes de thym régulièrement et je terminerai en disant aider son prochain…
merci j’y vois enfin plus clair grace à cet article. c’est vrai que la science avance à grand pas mais lire les études scientifiques est trop incomprehensible. C’est trop pointu. Et ce qu’en rapportent les journalistes est souvent inexact.
merci pour votre intérêt. c’est bien mon souhait d’expliquer aux profanes même si parfois il faut bien employer un vocabulaire un peu scientifique.